荧光(Fluorescence)是一种光致发光的物理现象。其核心原理是物质分子吸收高能量的光子后,电子发生能级跃迁,随后在极短时间内释放出低能量光子的过程。
荧光产生的三个阶段
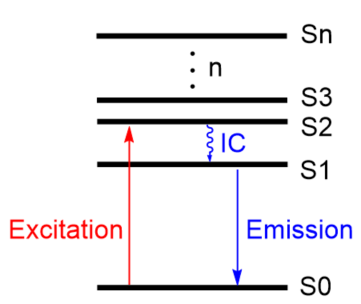
激发(Excitation):
当分子受到外来光源(如紫外线或蓝光)照射时,分子中的电子吸收能量,从能量较低的基态(S0)跃迁到能量较高的激发态(S1或S2,或者更高能级)。
非辐射跃迁(Non-radiative transition):
由于电子在激发态并不稳定,它会先通过非辐射跃迁的方式(如内转换 Internal Conversion,IC),迅速放出掉一部分能量后到第一激发态的最低振动能级(S1)。
发射(Emission):
电子从第一激发态返回基态时,剩余的能量以光的形式释放出来。由于在第二阶段损失了部分能量,释放出的光子能量比吸收时低,因此波长更长。
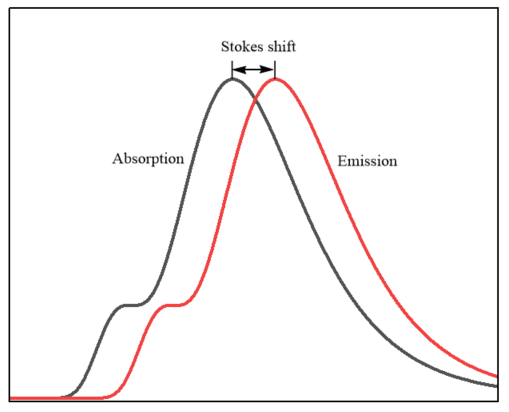
斯托克斯位移(Stokes Shift)
荧光最重要的特性是:发射光的波长总是长于激发光的波长。
例子: 物质吸收了高能的紫外线(不可见),发出的却是低能的绿光或红光(可见)。这种激发波长与发射波长之间的波长差被称为斯托克斯位移。
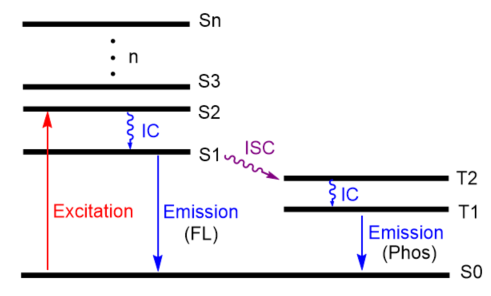
荧光和磷光的区别
这两者很多人容易混淆,其实主要区别在于电子跃迁的性质和持续时间:荧光是电子从S1跃迁回S0,持续时间极短(10-9 - 10-8秒),不会涉及电子自旋的改变。
磷光是电子从T1跃迁回到S0,持续时间较长(几秒到几小时),涉及电子自旋改变(一般通过系间窜越(Intersystem Crossing,ISC)由激发态单重态跃迁到三重态)。
 芯耀
芯耀



 3233
3233